История борьбы человека с болью уходит своими корнями в глубь веков, к эпосу героических сказаний прошлого, к древним мифам и полузабытым преданиям. По пути ошибок, неудач, случайных наблюдений, мистических и религиозных заблуждений и наряду с ними — эпохальных открытий шло наступление на боль. И лишь в XIX в., сметая противодействие, фанатизм, невежество, косность, традиции и привычки, — наметились контуры полной победы над болью и медицина подошла к решению самой трудной задачи проблемы обезболивания — к возможности регулировать болевое восприятие (Кассиль Г.Н., 1975).
Понимание отличий между разными типами боли важно для правильной ее терапии. Так, например, по продолжительности боль можно разделить на острую и хроническую. Последняя в свою очередь классифицируется в зависимости от источника: ноцицептивная боль (nociceptive pain) — возникает при непосредственном воздействии повреждающего фактора на периферические болевые рецепторы (ноцицепторы) различных органов и тканей при их повреждении; нейропатическая боль (neuropathic pain) — это вид боли, который в отличие от обычной возникает не вследствие реакции на физическое повреждения, а в результате патологического возбуждения нейронов в периферической или центральной нервной системе, отвечающих за реакцию на физическое повреждение организма (обычную боль); висцеральная боль (visceral pain) — боль, возникающая во внутренних органах; смешанная боль, которая имеет смешанное происхождение (схема1).
В настоящее время купирование боли в значительной степени достигается за счет применения так называемых традиционных обезболивающих препаратов, которые представлены рядом лекарственных средств разных классов2, таких как ацетаминофен, наркотические анальгетики, ацетилсалициловая кислота, метамизол натрия и пр. Они продолжают оставаться основными средствами, применяющимися для купирования болевого синдрома. Однако несколько позже к терапии боли были привлечены лекарственные средства из других фармакотерапевтических групп, такие как антидепрессанты, противоэпилептические средства и препараты из группы селективных ингибиторов циклооксигеназы-2 (ЦОГ-2). Доля последних на фармацевтическом рынке развитых стран в связи с побочными эффектами со стороны, например, сердечно-сосудистой системы, начиная с 2004?г. стала уменьшаться в пользу нестероидных противовоспалительных препаратов (НПВП), представленных неселективными ингибиторами ЦОГ, и опиатов.
Несмотря на то что имеющиеся в распоряжении современной медицины обезболивающие средства эффективны у большинства больных, тем не менее лишь 1 из 4 пациентов, принимающих эти препараты, достигают при этом адекватного облегчения боли. В настоящее время среди обезболивающих средств также зачастую отмечается плохая переносимость, довольно часто наблюдаются побочные эффекты, возникают проблемы, касающиеся их долгосрочной безопасности и злоупотребления, а также отмечается неудобство применения (Woodcock J., 2009). Это свидетельствует о том, что современная медицина продолжает испытывать потребность в новых эффективных и безопасных препаратах для купирования болевого синдрома.
О рынке обезболивающих средств развитых стран, а также стратегиях, направленных на удовлетворение потребности в данной нише, рассказал один из материалов, опубликованных недавно в журнале «Nature Reviews Drug Discovery». В нем рассматриваются стратегии по восполнению недостатка обезболивающих лекарственных средств. Во-первых, это изменение состава (reformulation) обезболивающего препарата и способов доставки действующего вещества; во-вторых, это расширение показаний к применению уже существующих препаратов из других фармакотерапевтических групп, которые ранее не использовались в качестве обезболивающих средств, а также применение препарата у определенной популяции пациентов, проявляющей к нему специфичную чувствительность; наконец, в-третьих, — это разработка инновационных лекарственных средств с совершенно новым механизмом действия.
| БОЛЬ | ||||||||||
 |
 |
|||||||||
| Острая боль | Хроническая боль | |||||||||
 |
 |
|
|
|
||||||
| ноцицептивная боль | нейропатическая боль | висцеральная боль | смешанная боль | |||||||
 |
 |
 |
 |
 |
||||||
| центральная | периферическая | |||||||||
 |
 |
|||||||||
| – травма, повреждение- послеоперационная боль | – остеоартрит (16 млн человек)- ревматоидный артрит (2,5 млн человек) | – рассеянный склероз- повреждение спинного мозга
– мигрень (31 млн человек) |
– постгерпетическая невралгия (0,11 млн человек)- диабетическая невропатия (3,2 млн человек) | – панкреатит- синдром раздраженного кишечника | – рак (1,5 млн человек)- фибромиалгия (6 млн человек) |
|||||
Классификация боли и типичные симптомы (в скобках указана распространенность того или иного вида боли среди пациентов в США)
ПРЕПАРАТЫ С ИЗМЕНЕННЫМ СОСТАВОМ
Многие фармацевтические компании прибегают к тому, что меняют состав уже существующих обезболивающих средств, вводя в их рецептуру активные фармацевтические ингредиенты, которые в течение сравнительно длительного времени уже маркетировались на рынке и продемонстрировали свою эффективность и безопасность. Эта идея не нова и используется на фармрынке не один десяток лет. Возьмем в качестве примера хотя бы ставший традиционным препарат Цитрамон: он включает комбинацию ацетилсалициловой кислоты и парацетамола и/или кофеина — препаратов, оказывающих обезболивающее действие. Подобный подход в создании препаратов значительно снижает риски компании, связанные с развитием нового продукта (например недостаточная эффективность или побочные эффекты, выявленные в ходе его изучения), а также его стоимость, — в итоге препарат с измененным составом все равно будет стоить дешевле по сравнению с инновационным продуктом. Собственно, большинство новых лекарственных средств, одобренных к маркетингу в последние годы, являются ни чем иным, как препаратами с измененным составом.
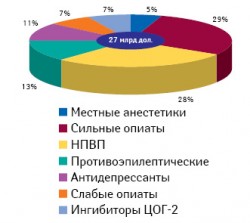
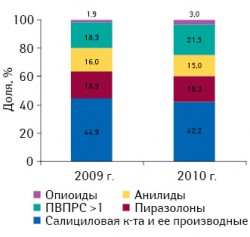
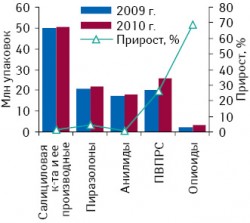
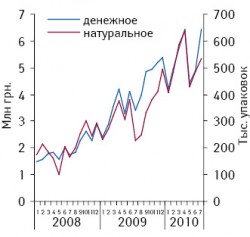
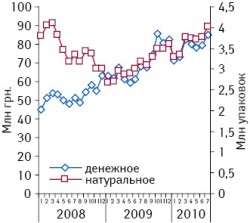
Препараты группы наркотических анальгетиков считаются одними из самых давних и самых эффективных в терапии выраженной боли. Этот класс лекарственных средств составляет наибольшую долю среди обезболивающих препаратов, представленных на фармрынке развитых стран в 2009?г., — 29%, или около 7,83?млрд дол. (рис. 13). На украинском фармацевтическом рынке доля этой группы препаратов ничтожно мала, а объем продаж препаратов из группы наркотических анальгетиков (N02A «Опиоиды») в денежном выражении в 2009?г. составил 48,15?млн грн. (почти 6,1?млн дол.). Можно предположить, что причиной тому — наличие в Украине слишком сложных и жестких механизмов назначения и отпуска наркотических анальгетиков, а также контроля за этими препаратами, что неоправданно затрудняет доступ к ним. Так, за 7?мес 2009–2010?гг. удельный вес группы наркотических анальгетиков в общем объеме продаж обезболивающих препаратов в натуральном выражении составил 1,9?и 3% соответственно (рис. 24), тогда как прирост за этот же период в 2010?г. составил 68,6% (рис. 34). За 7?мес 2010?г. объем продаж наркотических анальгетиков составил 37,05?млн грн. за 3,65?млн упаковок; динамика объема продаж опиоидов за январь 2008 — июль 2010?гг. приведена на рис. 44.
Однако, кроме серьезных побочных эффектов, как, например, угнетение дыхательной функции, главная проблема, связанная с применением наркотических анальгетиков, касается риска развития наркотической зависимости, пристрастия, привыкания и злоупотребления этими препаратами. Именно поэтому в феврале 2009?г. Управление по контролю за пищевыми продуктами и лекарственными средствами США (Food and Drug Administration — FDA) объявило, что потребует от фармацевтических компаний, занятых в производстве лекарственных средств с высоким содержанием опиатов, осуществить разработку стратегии по оценке и снижению рисков (Risk Evaluation and Mitigation Strategies) (Woodcock J., 2009). Подобная политика в отношении наркотических анальгетиков, как ожидается, должна сыграть позитивную роль в разработке новых форм препаратов, например, с пролонгированным высвобождением действующего вещества, а также лекарственных форм, предотвращающих злоупотребление препаратом (abuse-deterrent formulations) (к примеру заключение наркотического анальгетика в микрокапсулу с нерастворимой оболочкой). В качестве примеров можно привести недавно одобренный в США препарат, содержащий оксикодон с контролируемым высвобождением действующего вещества, под торговым наименованием OxyContin™ компании «Purdue Pharma L.P.», а также комбинированное средство морфина и налтрексона, известное под торговым наименованием Embeda™ компании «King Pharmaceuticals Inc.». Ожидают одобрения в США также несколько препаратов-кандидатов, например Remoxy™ компаний «King Pharma» и «Pain Therapeutics Inc.», представляющий собой препарат оксикодона пролонгированного действия, и Acurox™ (оксикодон+ниацин, «King Pharma»/«Acura Pharmaceuticals Inc.»). Правда, вероятность одобрения Acurox в ближайшее время приобрела несколько нечеткие формы из-за того, что в апреле 2010?г. эксперты FDA голосами 19:1?высказались против выдачи разрешения не маркетинг данного препарата.
Среди побочных эффектов обезболивающих средств нам также хорошо известен риск желудочно-кишечных кровотечений при применении неселективных ингибиторов ЦОГ из группы НПВП (Woodcock J., 2009). Поэтому в настоящее время разрабатывается несколько лекарственных средств, представляющих собой комбинацию неселективного ингибитора ЦОГ и препарата с гастропротекторным действием в одной таблетке. Например, в FDA уже рассмотрена маркетинговая заявка на одобрение препарата Vimovo™, разработанного компаниями «Pozen Inc.» и «AstraZeneca plc», который представляет собой комбинацию ингибитора протонной помпы эзомепразола с напроксеном; вторая заявка касается комбинации антагониста Н2-гистаминовых рецепторов фамотидина с ибупрофеном в составе препарата Duexa™ компании «Horizon Pharma Inc.». Как показали клинические исследования обоих средств, их применение у пациентов с артритом легкой и средней степени тяжести значительно снижало риск развития желудочно-кишечных язв (www.astrazeneca.com; www.fdanews.com).
РАСШИРЕНИЕ ПОКАЗАНИЙ
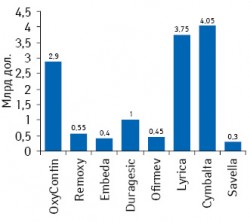
Антидепрессант Cymbalta™ (дулоксетин, «Eli Lilly&Co. Inc.») и антиконвульсант Lyrica™/Лирика (прегабалин, «Pfizer Inc.»), кроме своих основных показаний, были одобрены FDA также и для купирования различных типов нейропатической боли и фибромиалгии (Arnold L.M., 2009; Dworkin R.H., O’Connor A.B., Audette J. et al., 2010). Милнаципран, который первоначально был одобрен в 1980-х годах в Европе для лечения депрессии, был развит в качестве препарата для терапии фибромиалгии компаниями «Forest Laboratories Inc.» и «Cypress Bioscience Inc.» под торговой маркой Savella™ и выведен на фармрынок США в 2009?г. Все перечисленные выше продукты способствовали увеличению объема рынка обезболивающих средств за последние несколько лет. Расширение показаний к применению препаратов, касающиеся купирования боли, приведет к дальнейшему увеличению рынка обезболивающих средств. Ежегодный объем продаж некоторых из названных препаратов в развитых странах в 2009?г. приведен на рис. 55 (объемы продаж Lyrica и Cymbalta относятся к продажам по всем одобренным показаниям; для лечения нейропатической боли и фибромиалгии эти препараты назначаются в 30–35 и 20–25% случаев соответственно (Melnikova I., 2010)).
Объемы продаж продуктов, относящихся к отечественному рынку обезболивающих препаратов, были показаны на рис. 3. Сюда мы отнесли препараты группы М01 «Противовоспалительные и противоревматические средства» (кроме комбинаций с кортикостероидами и группы М01С «Специфические противоревматические средства»), которые в рисунках сокращенно названы ПВПРС, и подгруппы препаратов из группы N02 «Анальгетики», а именно: N02A «Опиоиды», N02В A «Салициловая кислота и ее производные» (кроме комбинаций с психолептиками), N02В В «Пиразолоны» (кроме комбинаций с психолептиками), N02В Е «Анилиды» (кроме комбинаций с психолептиками). В группе препаратов салициловой кислоты и ее производных, представленной такими продуктами, как, например, ацетилсалициловая кислота, отмечается «немедицинская» сезонность продаж, пики которых приходятся в основном на летние месяцы (июль–август). Она связана с сезонным приготовлением консервации овощей и фруктов (рис. 64). По состоянию на конец июля 2010?г. объем продаж этой группы препаратов в текущем году составил в денежном выражении 66,7?млн грн. (57?млн грн. — за аналогичный период 2009?г.), в натуральных показателях — 50,2?млн упаковок (49,7?млн упаковок — за 7?мес 2009?г.) (см. рис. 3). Как показано на рис. 2, удельный вес этой группы среди всех обезболивающих средств за 7?мес 2010?г. сократился на 2,7% по сравнению с 2009?г. Тем не менее она по-прежнему остается лидером, занимая самую большую долю рынка обезболивающих препаратов — 42,2%.
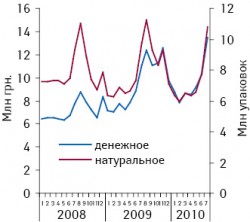
Более уравновешенной остается динамика объема продаж препаратов производных пиразолона, ярким представителем которой является метамизол натрия (рис. 74). За 7 мес 2010?г. объем продаж данной группы препаратов рос в основном в денежном выражении, составив 89,71 млн грн., что на 27,6% больше, чем за аналогичный период предыдущего года. В натуральном выражении за 7 мес 2010?г. объем продаж препаратов пиразолона увеличился на 4,4% до 21,8? млн упаковок по сравнению с 20,88 млн упаковок за аналогичный период предыдущего года (см. рис. 3). Доля этой группы препаратов в общем объеме обезболивающих средств практически осталась неизменной, в 2010?г. уменьшившись по сравнению с предыдущим годом на 0,6% (см. рис. 2). Эта группа средств оставила за собой третью по величине долю рынка обезболивающих препаратов, уступив в 2010?г. свое второе место препаратам группы ПВПРС.
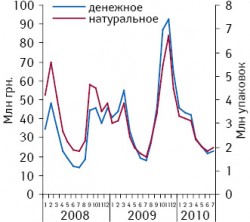
Если в случае с препаратами из группы салициловой кислоты и ее производных наблюдались сезонные колебания, пики которых приходились на летние месяцы, в группе производных анилидов (представлена, например, ацетаминофеном и фенацетином) наблюдается картина с точностью до наоборот (что вполне логично и объяснимо) (рис. 84). Пики объемов продаж этой группы, занимающей четвертую по величине долю среди всех обезболивающих препаратов, приходятся в основном на осенне-зимний сезон (октябрь–январь). Объем продаж этой группы препаратов за 7?мес 2010?г. в денежном выражении составил 230,7?млн грн., что на 2,4% меньше по сравнению с аналогичным периодом 2009?г., тогда как в натуральном выражении этот показатель за 7?мес 2009–2010?гг. незначительно увеличился (на 0,8%) с 17,65?до 17,8?млн упаковок (см. рис. 3).
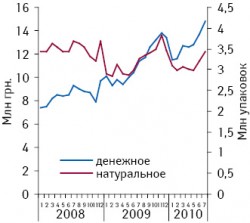
По итогам 7 мес выручка от реализации препаратов из группы ПВПРС увеличилась на 24%; примерно такой же прирост был зафиксирован и для объема продаж обезболивающих препаратов этой группы в натуральных показателях — 26% (рис. 94; см. рис. 3). Таким образом, можно сказать, что количество реализованных упаковок этой группы препаратов вернулась к докризисным объемам. В удельном весе данная группа по итогам 7?мес 2010?г. заняла второе место среди всех обезболивающих средств, сдвинув на третье место препараты группы пиразолонов (см. рис. 3).
ПРЕПАРАТЫ С НОВЫМ МЕХАНИЗМОМ ДЕЙСТВИЯ
В течение многих столетий боль рассматривалась в качестве симптома, сопровождающего какое-то основное заболевание. Именно поэтому терапия боли была направлена именно на купирование проявлений данного симптома вместо лечения первопричины, вызывающей боль. Только совсем недавно было выяснено, что боль, в частности хроническая, может существовать как самостоятельное заболевание. Ученые также продвигаются в понимании молекулярных механизмов боли, что позволяет им разрабатывать анальгетические препараты, воздействующие на несколько звеньев механизма ее развития.
Например, фактор роста нервов (англ. nerve growth factor — NGF) играет важную роль в генерировании боли и развитии гиперальгезии. Ингибирование NGF является одним из новых подходов в разработке обезболивающих лекарственных средств. Несколько NGF-специфических антител в настоящее время проходят клинические исследования II/III фазы, включая такие препараты-кандидаты, как танезумаб («Pfizer»), SAR164877/REGN475 («sanofi-aventis S.A.»/«Regeneron Pharmaceuticals Inc.»), а также JNJ-42160443/AMG403 («Johnson&Johnson Pharmaceutical R&D»/«Amgen Inc.»). В случае если танезумаб будет одобрен, как это планируется в 2012?г., он станет первым биологическим средством для лечения хронической боли и может стать первым препаратом, который будет одобрен преимущественно для лечения поясничной боли.
Глиальные клетки обещают стать новой мишенью в лечении хронической нейропатической боли. Так, модуляторы глиальных клеток, использующиеся в комбинации с опиатами, помогут повысить эффективность наркотических анальгетиков, а также помочь избавиться от наркотической зависимости и развития привыкания к этой группе лекарственных средств. Несколько препаратов — модуляторов глиальных клеток в настоящее время находятся на ранней стадии клинического развития: препарат-кандидат SLC022?компании «Solace Pharmaceuticals Inc.» в настоящее время проходит IIa фазу, а неубластин компании «Biogen Idec Inc.» — I фазу клинических испытаний.
Вследствие высокой обеспокоенности FDA соотношением польза/риск у анальгетиков с новыми механизмами действия показания к применению этих препаратов будут специфическими и узконаправленными, считают эксперты (Melnikova I., 2010). Однако при этом, учитывая востребованность данной группы препаратов, даже небольшая их доля на фармацевтическом рынке предоставит компаниям прекрасные коммерческие возможности.
Но поскольку боль — сложное явление, в развитии которого имеется несколько механизмов, то, вероятно, просто одним препаратом, пусть даже инновационным и с новым механизмом действия, полностью справиться с ней будет сложно. Поэтому более рациональным для купирования боли является терапия на основе комбинации нескольких лекарственных средств, действие которых направлено на блокаду ключевых периферических и центральных механизмов ее возникновения.
Мировой фармацевтический рынок обезболивающих средств в 2009 г. оценивался в более чем 50 млрд дол., включая 27 млрд дол., которые приходятся на экономически развитые страны, такие как США, Япония, Франция, Германия, Италия, Испания и Великобритания (см. рис. 1). Увеличение продолжительности жизни населения планеты, рост численности хронических заболеваний, одобрение новых продуктов из группы анальгетиков, а также повышение уровня образования врачей и знаний пациентов относительно доступных способов терапии — все это будет способствовать дальнейшему росту и развитию рынка обезболивающих средств. Примером постоянных инноваций в сегменте является глобальный лонч препарата Аркоксия® (Arcoxia®) компании «MSD» в этом году. Примечательно, что в Украине данный препарат появился одновременно с выходом на мировые рынки.
Однако вследствие наличия на фармрынке множества генерических версий препаратов-анальгетиков и их невысокой стоимости по сравнению с оригинальными препаратами лишь небольшое число новых лекарств достигнет статуса блокбастера (продажи которых превышают 1 млрд дол., как, например, у OxyContin (см. рис. 5). Таким образом, новые обезболивающие средства, которые будут одобрены в ближайшем будущем, вряд ли смогут вытеснить любой из продуктов, маркетирующихся на рынке в настоящее время, а также, вероятнее всего, будут показаны к применению среди узкого и специфического круга пациентов. А значит, большинство из нас еще в течение продолжительного времени будут использовать основную массу хорошо известных и доступных обезболивающих препаратов.
по материалам журнала «Nature Reviews Drug Discovery»;
www.iasp-pain.org; moz.gov.ua; www.nejm.org;
www.fda.gov; www.amjmed.com
1 Источники: Центр по контролю и профилактике заболеваний США (Centers for Disease Control and Prevention), Национальный центр статистики здравоохранения США (National Center for Health Statistics), Фонд артрита США (Arthritis Foundation), Национальный институт диабета, болезней пищеварительной системы и почек США (National Institutes of Diabetes and Digestive and Kidney Diseases), Американское общество боли, Американский фонд боли (American Pain Foundation).
2 Представлены группами препаратов M01 «Противовоспалительные и противоревматические средства» (далее — ПВПРС) и N02 «Анальгетики» по АТС-классификации.
3 Источники: «Datamonitor Group», «IMS Health Inc.», «Decision Resources Inc.».
4 По данным системы исследования рынка «Фармстандарт»/«PharmXplorer» компании «Proxima Research».
5 За исключением препаратов Remoxy и Ofirmev, которые не маркетируются на рынке США по данным показаниям: новая заявка на одобрение Remoxy, вероятно, будет представлена в FDA в IV кв. текущего года, а Ofirmev, как ожидается, будет одобрен только в III кв. 2010 г.




Коментарі