Итоги дебатов в Совете Европы
Министры – члены Совета Европейского Союза (Council of the European Union) обсудили вопрос о том, может ли возвращение производства лекарственных средств обратно в ЕС смягчить проблемы с их поставками. Ранее (26 ноября) с открытым письмом к Европейской комиссии с просьбой уделить приоритетное внимание решению проблемы нехватки лекарств обратился исполнительный комитет «Medicines for Europe» (Лекарственные средства для Европы), бывшей Европейской ассоциации производителей генерических лекарственных средств (European Generic Medicines Association – EGA).
Рыночные сбои, высокие цены и политика
Состоялось данное мероприятие по инициативе Генерального секретариата Совета (General Secretariat of the Council – GSC), назвавшего предотвращение нехватки имеющим «решающее значение для обеспечения непрерывности медицинской помощи». В заявлении GSC, датированном 22 ноября, отмечено, что нехватка стала отчасти результатом «более длинной, более сложной и фрагментированной» цепочки поставок, «поскольку компании разместили большую часть производства лекарств за пределами ЕС».
В настоящее время недостаточные поставки и уход с рынка «старых» лекарств создают риск для безопасности пациентов и увеличивают загруженность медицинского персонала. Кроме того, пациенты в ЕС по-прежнему имеют разные уровни доступа к новым препаратам из-за рыночных сбоев, высоких цен и маркетинговых стратегий компаний.
Представлен также взгляд на проблему жизненного цикла лекарств, состоящего из четырех фаз (рисунок):
1) исследования и разработка (R&D): на этом этапе стимулы в виде национальных и европейских финансовых инструментов играют важную роль;
2) новые лекарства: на этом этапе важны пострегистрационные стимулы (защита данных, рыночная эксклюзивность), контролируемое внедрение и достижение равного доступа;
3) ценовая конкуренция: на этом этапе решающее значение имеет хорошо функционирующий рынок;
4) «старые» лекарства: на этом этапе важными целями являются поддержание лекарств на рынке и контроль их нехватки.
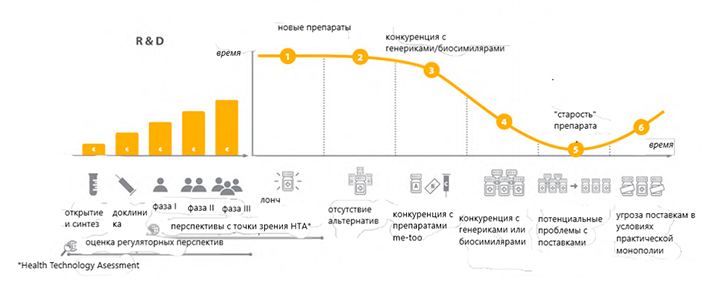
В числе проблемных моментов отмечены неравное положение стран-членов в отношении возможности обеспечения равного доступа (компании выводят препараты на рынки разных стран в разное время, несмотря на одобрение по централизованной процедуре), уязвимость чрезмерно длинных и фрагментированных цепочек поставок и неконтролируемое прекращение поставок «старых» лекарств, вынуждающее системы здравоохранения пользоваться более дорогими и/или менее эффективными альтернативами.
Координация действий
В документе, резюмирующем итоги дебатов, состоявшихся 9–10 декабря 2019 г., отмечено, что целью дискуссии было обсуждение решений постоянной проблемы обеспечения доступа к лекарственным средствам в ЕС. Были, в частности, выделены несколько возможных мер для обеспечения более легкого доступа к лекарственным средствам:
– поощрение перемещения производства лекарств обратно в ЕС;
– перемещение лекарств из одного государства-члена в другое с некоторыми исключениями относительно требований к сопровождающей их информации;
– обмен данными о запасах;
– использование механизмов раннего предупреждения о проблемах с поставками;
– усиление надзора за рынком;
– укрепление сотрудничества на уровне ЕС.
Большинство делегатов из разных государств-членов «поддержали идею разработки и реализации программы ЕС по фармацевтической политике, направленной на предотвращение нехватки лекарств во всем ЕС», отмечено в резюмирующем документе.
По материалам www.consilium.europa.eu

Коментарі
Коментарі до цього матеріалу відсутні. Прокоментуйте першим