Віддача від інвестування в інновації
Як свідчить аналіз консалтингової компанії Deloitte, який враховує 20 найбільших біофармацевтичних компаній, протягом 2013–2022 рр. відзначали зниження середнього показника внутрішньої норми рентабельності (internal rate of return — IRR) активів на пізній стадії розробки. Винятком цієї тенденції став сплеск у 2021 р., зумовлений розробкою вакцин для профілактики COVID-19, після чого IRR знову суттєво знизився. Однак протягом останніх 2 років відмічають зростання цього показника, й у 2024 р. він становив 5,9% (рис. 1).
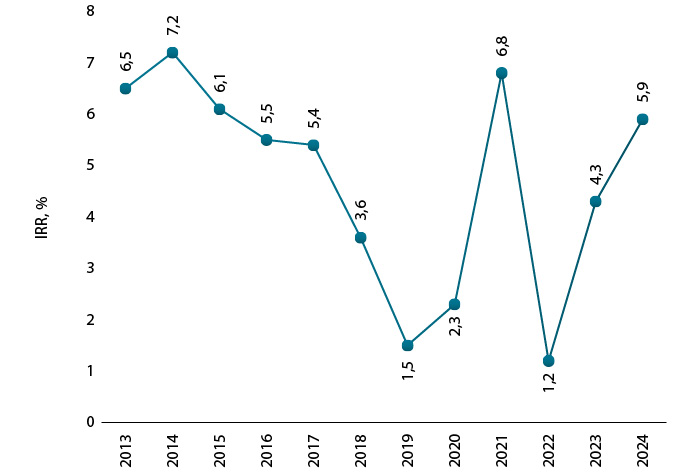
Ця позитивна тенденція може бути обумовлена збільшенням кількості потенційно дороговартісних кандидатів у препарати та/або блокбастерів, які переходять на пізню стадію R&D, у тому числі в терапевтичних сферах з великими незадоволеними медичними потребами. Однак витрати на дослідження та розробку залишаються високими, а складність і конкуренція зростають. Середня вартість розробки у 2024 р. оцінюється на рівні 2,2 млрд дол. США (рис. 2).
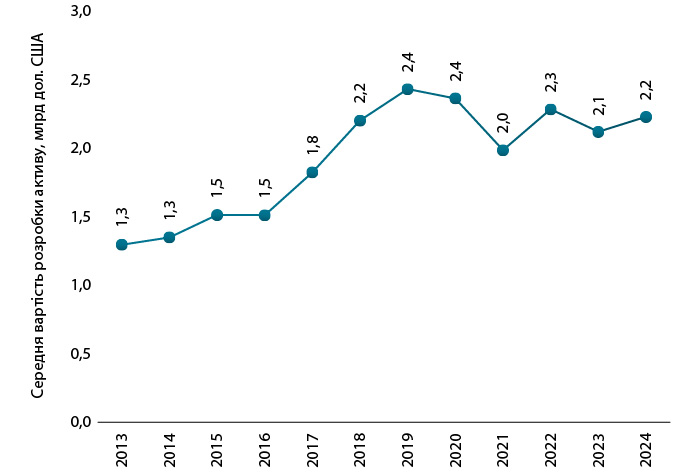
Вища потенційна прибутковість є важливим фактором. Дані Deloitte свідчать про те, що кількість особливо прибуткових інноваційних кандидатів у препарати помітно збільшується. Так, у 2024 р. у пізню стадію перейшло 29 кандидатів у препарати, які після лончу можуть генерувати річний дохід понад 1 млрд дол., порівняно з 19 у 2023 р.
Ще однією важливою тенденцією є уповільнення зростання витрат на R&D за останні 5 років, що зумовлено, зокрема, підвищенням ефективності та прискоренням досліджень і розробок. Тому рішення зосередитися на цьому аспекті цілком виправдане.
Хоча фармацевтичні компанії прагнуть диверсифікувати свої продуктові портфелі, велика кількість R&D-проєктів сконцентрована на активах для лікування онкологічних захворюваннь, а також інфекційних хвороб. Стратегічною можливістю для фармкомпаній може стати концентрація зусиль на менш насичених терапевтичних сферах. Вихід у ніші з обмеженими варіантами лікування може надати конкурентну перевагу та відкрити нові перспективи для інновацій.
Розробка кандидатів у препарати з новим механізмом дії має ключове значення для довгострокового зростання. Після лончу такі лікарські засоби можуть забезпечити значно вищий дохід. Попри високі ризики, освоєння нових напрямків є критично важливим для розробки проривних методів лікування з кращими результатами для пацієнтів. Така стратегія сприяє також досягненню вищого показника IRR.
Стратегічні M&A
З наближенням втрати ексклюзивності оригінальних препаратів, особливо блокбастерів, з метою захисту потоку доходів фармацевтичні компанії можуть укладати угоди зі злиття та поглинання (mergers and acquisitions — M&A), поповнюючи свій продуктовий портфель новими перспективними активами. Помітною тенденцією є відхід від мегаугод до менш масштабних транзакцій та придбання активів на ранніх стадіях розробки.
Штучний інтелект
Біофармацевтична галузь переживає справжню цифрову трансформацію, впроваджуючи новітні технології, зокрема штучний інтелект (ШІ), для прискорення R&D-процесів і підвищення їхньої продуктивності. За прогнозами Deloitte, до 2030 р. ШІ, включаючи великі мовні моделі, а також передові методи редагування генів, зможуть суттєво прискорити відкриття персоналізованих та економічно ефективних методів лікування. ШІ та великі мовні моделі можуть прискорити відкриття завдяки їх можливостям щодо моделювання білкових структур, аналізу бібліотек молекул з метою виявлення перспективних кандидатів у препарати та перепрофілювання лікарських засобів, а також забезпечити моніторинг даних клінічних випробувань у режимі реального часу.
Поєднання ШІ з потужними обчислювальними технологіями сприятиме оптимізації дизайну клінічних випробувань, генерації даних і автоматизації звітності. Використання ШІ у клінічних випробуваннях може покращити відбір учасників, моніторинг і аналіз даних, що зрештою дасть змогу скоротити терміни розробки нових препаратів.
Жіноче здоров’я
За даними консалтингової компанії McKinsey, в клінічних випробуваннях «жіноче здоров’я» часто розглядалося лише через призму репродуктивних органів, ігноруючи інші критичні біологічні відмінності, такі як клітинна стать (не тільки людина має стать, але й кожна клітина тіла також має стать), гормональний вплив тощо.
Попри те що жінки зазвичай живуть довше за чоловіків, вони проводять на 25% більше часу в стані поганого самопочуття або здоров’я (poor health) порівняно з чоловіками, що може бути зумовлено частково відсутністю врахування статі під час розробки препаратів. Усунення цієї прогалини може покращити результати для здоров’я та якість життя жінок, а також додати щонайменше 1 трлн дол. до світової економіки у 2040 р.
Розрив у показниках здоров’я між жінками та чоловіками може бути зумовлений кількома ключовими факторами. Серед них — недостатнє розуміння біологічних відмінностей між статями, недооцінка специфічних симптомів захворювань у жінок, брак клінічних даних із гендерним розподілом, а також недостатнє фінансування досліджень у сфері жіночого здоров’я.
Перспективи
Аналітики McKinsey, аналізуючи фундаментальні причини зниження продуктивності R&D протягом останнього десятиліття, відзначають основні з них — зниження ймовірності успіху, зростання вартості виведення на ринок нових препаратів та загострення конкуренції у сфері R&D. Фахівці виокремлюють декілька основних елементів R&D, які здатні підвищити ефективність і результативність розробки нових препаратів, включаючи спрощення управління, динамічний розподіл ресурсів, здійснення діяльності, що має високу цінність, власними силами та формування партнерства щодо інших видів діяльності.
Фахівці Deloitte теж визначають кілька ключових факторів, які можуть підтримати позитивну динаміку IRR в майбутньому. Серед них — фокус на терапевтичні напрями з високим рівнем незадоволених медичних потреб, зміщення уваги до захворювань, що потребують нових рішень, а також розробка препаратів із новими механізмами дії. Зазвичай такі препарати демонструють значно вищий потенціал прибутковості, а ідентифікація перспективних терапевтичних ніш є особливо важливою з огляду на необхідність компенсувати зменшення обсягів продажу після закінчення терміну патентного захисту оригінальних препаратів. Фокус на нові терапевтичні напрямки може надати такі переваги, як нижча конкуренція та пул пацієнтів, які потребують варіантів лікування. Коли ж більшість R&D сконцентровується навколо обмеженої кількості нозологій, конкуренція за ключові випробувальні центри та групи пацієнтів посилюється. Окрім того, зосередження зусиль на обмеженій кількості цілей може пригнічувати інновації й обмежувати потенційні можливості лікування для пацієнтів із незадоволеними медичними потребами.
Інвестиції в аналітику даних і інструменти ШІ теж відіграють не останню роль. Дуже важливо використовувати передові технології на свою користь. Збільшення інвестицій у технології редагування генів, а також R&D на базі ШІ сприятимуть прискоренню відкриття проривних методів лікування. Однак варто враховувати, що хоча завдяки ШІ можна підвищити ефективність, оптимізувати витрати на R&D та прискорити вихід лікарських засобів на ринок, очевидно, для отримання відчутних результатів знадобиться декілька років.
Використання реальних даних, розширеної аналітики та цифрових біомаркерів дає змогу ухвалювати більш обґрунтовані рішення на всіх етапах життєвого циклу R&D — від визначення терапевтичних цілей і розробки дизайну клінічних випробувань до відбору учасників випробувань та укладання стратегічно важливих M&A-угод.
за матеріалами http://www.deloitte.com,
http://www.mckinsey.com, http://www.sciencedirect.com

Коментарі
Коментарі до цього матеріалу відсутні. Прокоментуйте першим